Intelligence artificielle et nouvelles technologies pour le diagnostic et le suivi des pathologies rétiniennes
L’environnement numérique se développe sans cesse et nous apporte chaque jour de nouvelles possibilités d’aide au diagnostic, ou de proposition thérapeutique. L’ergonomie s’est améliorée afin de permettre une délégation complète des acquisitions aux orthoptistes. Mise au point automatique, eye tracker et enfin analyses semi-automatiques autorisent le maniement des OCT ou rétinographes sans l’ophtalmologiste. Tout converge donc aujourd’hui vers le déploiement de la télémédecine et l’usage de l’intelligence artificielle (IA) en ophtalmologie.
La télémédecine autorise, voire valorise le transfert de données sécurisées. L’IA propose une aide au diagnostic ou même une thérapeutique individualisée. L’association des 2 permettra de démocratiser et d’uniformiser sur le territoire les connaissances médicales autrefois limitées à certains centres experts.
La pandémie en cours n’est que le révélateur, à ce titre, d’une lame de fond amorcée il y a quelques années. Il y a, en raison du confinement, une prise de conscience des soignants mais aussi des patients sur les outils de santé connectés. Ces progrès s’imposent à nous et loin de les observer avec défiance, nous devons y être attentifs. Ils offrent en effet un gain de temps précieux compte tenu de l’inadéquation entre l’offre et la demande de soins visuels. Enfin, il faudra admettre les capacités supérieures de l’IA pour le diagnostic et la thérapeutique. L’enjeu des prochaines années sera, à coup sûr, de s’approprier ces technologies afin de les intégrer dans notre pratique clinique tout en proposant un modèle médico-économique pertinent.
Applications d’évaluation d’acuité visuelle et de suivi
L’utilisation grandissante des smartphones et des tablettes connectés chez les seniors permet d’envisager l’évaluation personnalisée de l’acuité visuelle (AV) et son suivi à domicile.
ForeseeHome représente une avancée dans la surveil-lance à domicile de la DMLA humide. L’appareil permet de réaliser quotidiennement un test simple pour vérifier les changements minimes dans la vision. Il est fondé sur le principe de la détection précoce des distorsions. Les rapports mensuels sont envoyés directement chez le médecin qui est alors alerté. Selon Querques et al., ForeseeHome a été plus sensible aux changements de la DMLA que les méthodes de tests à domicile plus anciennes telle la grille d’Amsler [1]. Le système bénéficie maintenant d’un agrément de la Food and Drug Administration (FDA) et se déploie aux États-Unis.
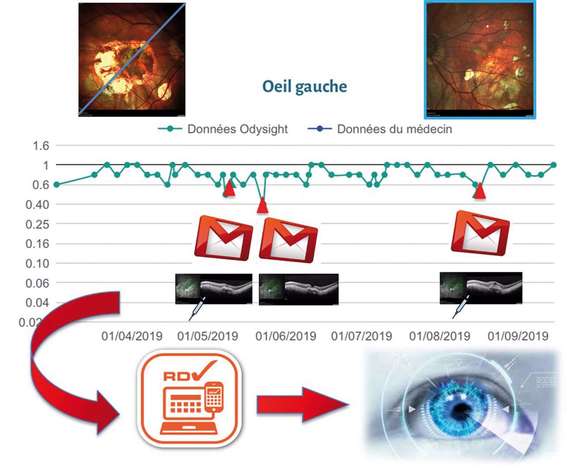
Dans le même esprit, l’application Odysight, de Tilak, a été lancée en 2019 pour le suivi des maculopathies : détecter précocement l’évolution de la maladie en générant une alerte de baisse d’AV pour anticiper la réponse thérapeutique (figure 1). L’application bénéficiant d’un marquage CE est probablement à ce jour la plus aboutie dans ce domaine. Un contrôle de la luminosité ambiante et de la distance de lecture permet une bonne reproductibilité des tests. L’accent est mis ici sur l’observance dont on sait qu’elle est faible pour les pathologies chroniques : déploiement via une prescription médicale et autotests liés à un jeu « addictif » de type Candy Crush. Les premiers résultats de notre cohorte de 60 patients sont prometteurs (en cours de publication). L’accueil est très favorable, en particulier pour les patients présentant un seul œil fonctionnel, un néovaisseau du myope fort ou des intervalles longs (supérieurs à 8 semaines) entre les injections intravitréennes (IVT). Le taux de conversion (mis en place après l’inscription dans le centre) et le taux de rétention (usage actif après le lancement) sont respectivement de 61 et de 38%, ce qui semble très favorable dans l’univers numérique. Les patients âgés de 50 à 70 ans et ceux qui jouent avec l’application représentent les plus actifs à 10 mois du lancement. Notre secrétariat a traité, en moins de 6 jours en moyenne, 15 alertes durant cette période. Il faut noter que la mise en place d’un nouvel outil numérique nécessite l’adhésion de toute l’équipe soignante afin d’informer et de motiver le patient, mais aussi de traiter les alertes à temps. Le cabinet se doit de fiabiliser l’ensemble de sa filière : du flux de patients connectés à la salle d’injection. L’application obtient un taux satisfaisant de détection avec une sensibilité de 87% et une spécificité de 98%. Bien entendu, l’isolement des patients et l’accès quasi impossible aux cabinets médicaux pendant l’épidémie de COVID-19 révèle l’intérêt de la surveillance à domicile. Le vécu des patients actifs est très satisfaisant pour ce service personnalisé. À l’inverse, certains se plaignent de son caractère « intrusif » ou de la fréquence des notifications. Ces paramètres, comme le signalement des alertes, devront être améliorés.
Même si aucun de ces systèmes n’est parfait, ils lancent, à coup sûr, les grandes lignes de ce que sera le suivi de nos patients. À l’heure actuelle, les patients de plus de 75 ans sont encore peu connectés. Nous développons des stratégies de suivi, de type Inject and Extend, pour alléger le suivi fastidieux et coûteux mais le cabinet médical reste le lieu de prise des décisions. Ces outils fiables et ergonomiques seront utilisés par les sexagénaires actuels déjà familiarisés aux nouvelles technologies et la pandémie ne fera qu’accélérer ce changement. Nous devrons probablement revoir nos organisations afin de recevoir les patients à bon escient en intégrant ces outils connectés (et leurs alertes) à nos agendas. Loin de redouter ces applications, la profession doit être leader dans leur déploiement. On constate, en effet, beaucoup plus de patients n’ayant pas accès à l’ophtalmologiste que de patients venant encombrer à tort nos salles d’attente. Toutefois, il est essentiel que l’ophtalmologiste reste le pivot du parcours visuel en étant seul informé d’une alerte... et pas le propriétaire ou diffuseur de l'application telle une mutuelle.
Des progrès constants
Du jeu de go à la reconnaissance des visages, de la traduction automatique au diagnostic médical, les progrès de l’IA sont exponentiels. Ils sont en grande partie liés à ceux de l’apprentissage profond (Deep Learning), qui donne aux machines la capacité d’apprendre à partir d’une grande quantité de données. L’ensemble des publications actuelles s’attache à montrer la non-infériorité de l’IA par rapport aux experts ; ainsi Deep Blue contre Garry Kasparov dans les années 1990. Nul doute que les prochaines évolutions verront la supériorité des algorithmes sur les capacités d’intégration humaines. L’IA permettra certainement des soins de santé personnalisés mais aussi une gestion à grande échelle [2].
Capacités actuelles et futures
- Détecter des anomalies : microanévrysme, hémorragie, dilatation veineuse, etc.
- Quantifier ces anomalies.
- Dépister et classifier des maladies.
- Guider la thérapeutique.
- Détecter des récidives.
- Établir des facteurs pronostiques.
Interprétation automatisée des rétinographies
Le smartphone (camera HD, lumière LED puissante) peut offrir un service inestimable grâce à sa connectivité (clinique ou téléophtalmologie) et à son faible coût comparé au prix d’un rétinographe, voire d’une lampe à fente. Une équipe indienne [3] a récemment publié une étude sur un nouveau téléphone intelligent (Fundus on Phone [FOP]) utilisé pour le dépistage de la rétinopathie diabétique (RD) comparé à un rétinographe classique. La photographie rétinienne acquise à l’aide de la caméra FOP était efficace pour le dépistage et le diagnostic de la rétinopathie et de la maculopathie diabétiques avec une sensibilité de 90% et une spécificité de 95% comparables aux photographies rétiniennes classiques.
Pour la première fois, la FDA a autorisé la mise sur le marché du robot IDx-DR doté d’une IA capable de diagnostiquer la RD. Après un apprentissage initial fondé sur une base de données française (Messidor-2), l’IA parvient désormais à détecter plus de 98% des cas de RD [4]. Le système est conçu pour automatiser le diagnostic sans la présence de l’ophtalmologiste qui perd son rôle central dans la filière. Il ne sera ainsi sollicité que par des patients préalablement diagnostiqués positivement par l’IA : perte de contrôle dans son recrutement ? Optimisation de la prise en charge ? Pour cela, les photographies sont envoyées vers un cloud qui héberge un algorithme répondant avec son diagnostic : soit il détecte une RD et invite le patient à consulter un ophtalmologiste, soit le résultat est négatif et l’algorithme propose un nouveau contrôle 1 an plus tard. Les résultats qui s’appuient sur 900 patients annoncent 87,4% de sensibilité et 89,5% de spécificité, comparables à 3 experts. À noter que près de 35% des clichés n’étaient pas interprétables par le robot contre 20% pour les experts.
Google, via sa branche Deep Mind [5], a développé un algorithme de détection de la RD avec une sensibilité de 96,1% et une spécificité de 93,9% (figure 2).
Enfin OphtAI, branche de la société française Evolucare, dispose elle aussi d’un algorithme très performant de détection automatique de la RD (sensibilité 99%, spécificité 87% en 3 secondes). Il possède le marquage CE et est intégré à une plateforme prometteuse pour le dépistage de la RD par télémédecine.
Interprétation automatisée des OCT
L’IA réussit maintenant à segmenter les liquides intra- et sous-rétiniens, les drusen, les décollements de l’épithélium pigmentaire, voire les atrophies géographiques (figure 3) [2]. Elle permet de détecter, avec une excellente précision, les différents types de liquide intrarétinien dans les maladies maculaires exsudatives telles qu’occlusion veineuse rétinienne, DMLA ou œdème maculaire diabétique [5].
Une équipe israélienne a montré que, une fois le diagnostic effectué, l’IA était capable, avec le logiciel NOTAL, de repérer les signes d’activité grâce à l’évolution et à la disposition du fluide [6]. Cet algorithme présente une sensibilité de 92% et une spécificité de 91% pour détecter les signes exsudatifs en OCT en comparaison avec 3 lecteurs rétinologues. Un OCT portable à domicile, couplé à l’IA, va être commercialisé, permettant de surveiller quotidiennement un patient et de l’adresser à l’ophtalmologiste en cas de besoin. La présence de fluide intrarétinien ayant été déterminée comme étant un facteur de pronostic péjoratif, l’appareil déclenche une alerte dès sa détection.
En collaboration avec l’institut d’ophtalmologie du University College de Londres et le Moorfields Eye Hospital (Londres), l’entreprise DeepMind de Google a montré en 2018 qu’un système d’IA pouvait recommander le diagnostic pour 50 maladies oculaires avec 94% de sensibilité (résultats comparables aux experts de l’étude) [7]. Surtout, elle a établi un classement des cas en fonction du degré d’urgence de la prise en charge pour chaque patient (figure 4).
Si les réseaux de neurones profonds obtiennent des résultats supérieurs, leur fonctionnement apparaît encore comme une « boîte noire » : on peut juger des données qui entrent dans la boîte et des résultats qui en sortent, mais sans savoir ce qui se passe à l’intérieur. Ces données (chiffres, images...) sont analysées par des couches successives de calculs qui attribuent à chaque fois un coefficient et transmettent le résultat à la couche suivante. Pour beaucoup de chercheurs, comme pour les pouvoirs publics, comprendre ces « boîtes noires », ou du moins rendre leur fonctionnement plus compréhensible, va devenir un enjeu juridique et éthique majeur. D’ailleurs, la déclaration de Montréal tente d’établir une charte pour un développement responsable de l’IA [8].
Nous ne sommes qu’au début du champ des possibles. Et lorsque l’on réalise qu’à partir d’une rétinophotographie, l’IA donne l’âge, le sexe, le statut de fumeur, la tension artérielle et le poids avec avec une marge d’erreur relativement faible, on mesure sa puissance potentielle (figure 5) [9].
Mais le modèle socio-économique reste à construire. Avec l’IA, l’unité de lieu et de temps de l’examen, du diagnostic et de la proposition thérapeutique disparaît. L’acquisition se déroule en un point, les données sont analysées à distance (possiblement à l’étranger), puis stockées sur des serveurs dans un troisième endroit… L’heure n’est plus à réfuter ni la rapidité ni la fiabilité des diagnostics fondés sur d’immense bases de données. Mais nous devons plutôt nous interroger : à qui vont appartenir ces machines « intelligentes », où seront stockées les données et comment, in fine, se fera la décision en accord avec la réglementation de chaque pays ? En France, pour répondre à la pénurie médicale, il serait tentant de diffuser ces analyses hors des cabinets médicaux. Mais alors qui paierait l’acte d’interprétation numérique ? Comment gérer les 25% de clichés ininterprétables ? À qui adresser ensuite les patients diagnostiqués ? Évoquons enfin l’abîme qui s’ouvre pour le patient avec son diagnostic numérique sans une prise en charge psychologique ou sociale indispensable associée.
L’IA intégrera probablement nos imageurs, nos logiciels métiers, voire des données plus larges du patient. Mais elle doit rester dans l’environnement médical pour éviter des dérives assurancielles ou financières.
Conclusion
Les nouvelles applications proposent des outils de suivi d’AV au domicile qui permettront, on l’espère, d’optimiser les contrôles au cabinet.
Le mythe de l’IA capable de reproduire les sentiments humains est encore loin mais force est de constater que les avancées récentes permettent d’ores et déjà une aide fiable et précise en ophtalmologie. Comme la plupart des systèmes d’IA dans le domaine de la santé, l’objectif n’est pas tant de remplacer l’ophtalmologiste que de lui fournir une capacité de décision la plus proche de celle que prendrait un expert. Souhaitons que l’ophtalmologiste conserve encore son diagnostic final, sa stratégie chirurgicale et sa vision horizontale de l’ensemble des problématiques d’un patient, mais surtout son empathie.
Nous devons être très attentifs à leurs évolutions et à leurs impacts dans la qualité de notre prise en charge médicale. De la réfraction autonome en passant par le diagnostic, le pronostic ou la suggestion de traitements, ces systèmes vont profondément modifier notre filière de soins.
Références bibliographiques
[1] Querques G, Querques L, Rafaeli O et al. Preferential hyperacuity perimeter as a functional tool for monitoring exudative age-related macular degeneration in patients treated by intravitreal ranibizumab. Invest Ophthalmol Vis Sci. 2011;52(9):7012-8.
[2] Schmidt-Erfurth U, Sadeghipour A, Gerendas BS et al. Artificial intelligence in retina. Prog Retin Eye Res. 2018;67:1-29.
[3] Rajalakshmi R, Subashini R, Anjana RM, Mohan V. Automated diabetic retinopathy detection in smartphone-based fundus photography using artificial intelligence. Eye (Lond). 2018;32(6):1138-44.
[4] Van der Heijden AA, Abramoff MD, Verbraak F et al. Validation of automated screening for referable diabetic retinopathy with the IDx-DR device in the Hoorn Diabetes Care System. Acta Ophthalmol. 2018;96(1):63-8.
[5] Schlegl T, Waldstein SM, Bogunovic H et al. Fully automated detection and quantification of macular fluid in oct using deep learning. Ophthalmology. 2018;125(4):549-58. [6] Chakravarthy U, Goldenberg D, Young G et al. Automated identification of lesion activity in neovascular age-related macular degeneration. Ophthalmology. 2016;123(8):1731-6.
[7] De Fauw J, Ledsam JR, Romera-Paredes B et al. Clinically applicable deep learning for diagnosis and referral in retinal disease. Nat Med. 2018;24(9):1342-50.
[8] www.montrealdeclaration-responsibleai.com/the-declaration
9] Poplin R, Varadarajan AV, Blumer K et al. Prediction of cardiovascular risk factors from retinal fundus photographs via deep learning. Nat Biomed Eng. 2018;2(3):158-64.